7 kroků proti ateroskleróze: Epigenetické tipy pro zdravé srdce a cévy

Dlouhá léta se v rámci prevence nemocí srdce a cév kladl důraz zejména na snižování hladiny cholesterolu a krevního tlaku. Jenže to jsou jen jedny z mnoha faktorů, které se podílejí na vzniku aterosklerózy. Možná ještě důležitější je třeba stav imunitního systému či míra zánětlivých procesů v těle. Co tedy pro svůj kardiovaskulární systém můžeme udělat z hlediska epigenetiky?
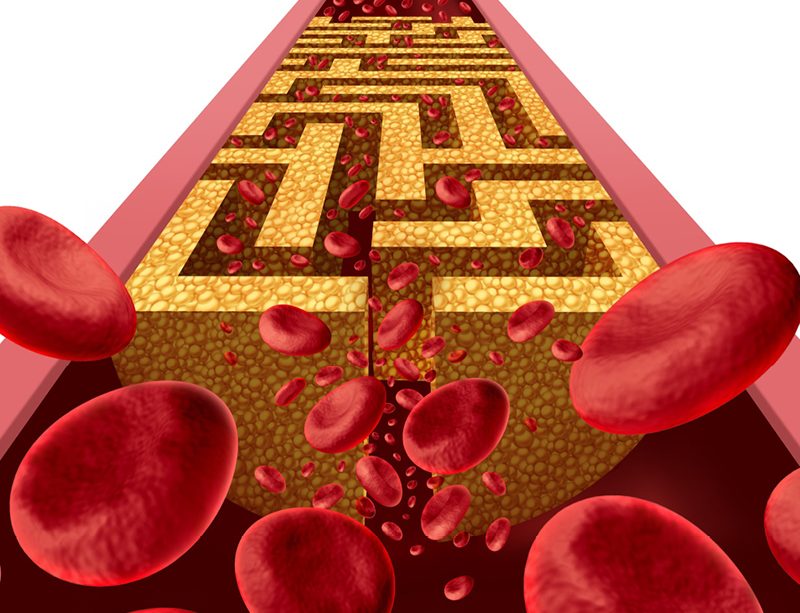
Kdysi to byly funkční cévy. Jejich stěna byla tenká a pružná, skvěle reagovala na potřeby tkání a podle toho zvyšovala či snižovala průtok krve, aby jim zajistila dostatek kyslíku a živin. Jenže teď vypadají úplně jinak. Z vnitřní strany cévní stěnu obklopuje silná vrstva usazených tuků, navíc vyztužená vápníkem. Průsvit cévy se tak snížil a krve tudy může protéct výrazně méně. A když srdce začne při rychlejším pohybu bušit jako o závod, není mu to nic platné. Tvrdé usazeniny nedovolí, aby se cévy roztáhly, a krve tudy protéká stále stejně. Co na tom, že tkáně křičí o nějaký ten kyslík navíc. Více krve se k nim nedostane a zoufalá snaha srdce ji tam napumpovat vede jen ke zvýšení krevního tlaku.
Takhle nějak se projevuje ateroskleróza, onemocnění cév, které je ve svém důsledku život ohrožujícím stavem. Způsobuje nejen ischemii, tedy nedostatečné zásobení kyslíkem, které může postihovat například srdeční svalovinu (tzv. ischemická choroba srdeční, dříve nazývaná angina pectoris), mozek, končetiny, ale v podstatě i jakoukoliv jinou část těla. Ještě horší je, že postižené cévy se mohou velice snadno ucpat, nebo dokonce prasknout. Pak nastává například infarkt myokardu (pokud to postihne cévu zásobující srdce) či mozková mrtvice (když k tomu dojde v mozku).
A to je nebezpečí, které není radno podceňovat – právě nemoci srdce a cév jsou totiž v západních zemích (včetně ČR) neohroženou jedničkou v žebříčku příčin úmrtí.
V hlavní roli zánět
Ateroskleróza je ve své podstatě především chronický zánětlivý proces podporovaný oxidativními procesy (tj. poškozením buněk volnými radikály). Na jejím počátku přitom stojí tzv. entoteliární dysfukce.
Entotel je vnitřní vrstva cév, která je velice aktivním orgánem důležitým pro rovnováhu procesů v cévách. Při dysfunkci se stává propustnější, dochází k narušení rovnováhy důležitých procesů, na cévní stěny se přichycují imunitní buňky jménem leukocyty a pronikají sem další imunitní buňky (makrofágy, monocyty, T-lymfocyty), které, pokud dojde k jejich aktivaci, podporují uvolňování prozánětlivých látek – zejména cytokinů a chemokinů. Negativní roli tu přitom mohou hrát i některé druhy infekcí.
Teprve na tyto procesy navazuje vlastní tvorba aterosklerotických plátů. Při ní nejprve dochází k přeměně imunitních buněk jménem makrofágy na tzv. pěnové buňky. Ty se pak v cévách hromadí a na jejich základě pak vznikají tukové proužky. Množství usazeného tuku posléze roste. Poté dochází k proliferaci (rychlému množení) buněk hladké svaloviny cévních stěn, nad nimiž vzniká kolagenová vazivová vrstva. Do těchto struktur se pak ukládá vápník, čímž dochází k jejich tvrdnutí. Ztvrdlé cévy pak mohou velice snadno praskat nebo se na jejich stěnách zachytávají krevní sraženiny.
Probudit ty správné geny
Existuje přitom celá řada genů, které se na procesu vzniku endoteliární dysfunkce a tvorbě aterosklerotických plátů podílejí. A na druhou stranu také celá řada genů, které nás před aterosklerózou chrání. Důležité přitom je, že aktivitu těchto genů lze ovlivnit, protože v našem těle neustále probíhají tzv. epigenetické reakce, které dokáží jednotlivé geny v naší DNA vypínat, nebo naopak zapínat.
Pokusy na myších například ukázaly, že pokud dojde k „vypnutí“ genů, podle nichž se v těle tvoří cytokiny podporující zánět (např. IL-12 nebo TNF-α), dojde u pokusných zvířat ke snížení výskytu aterosklerózy. A naopak, pokud jsou vypnuty geny pro tvorbu cytokinů protizánětlivých (např. IL-10), výskyt aterosklerózy se zvýší.
Z epigenetických reakcí je zde důležitá zejména tzv. metylace genů. Ukazuje se totiž, že pokud je DNA člověka nadměrně metylována, výrazně se zvyšuje riziko úmrtí na kardiovaskulární choroby. Roli však hraje i další důležitá epigenetická reakce, modifikace histonů (zejména pak histonu H4). Platí přitom, že acetylaci histonů může ovlivnit i přítomnost oxidovaného LDL cholesterolu.
Zajímavé přitom je, že některé epigenetické změny, které zvyšují riziko kardiovaskulárních chorob, přitom vznikají již v době nitroděložního vývoje, zejména pak v souvislosti se špatnou výživou matky.
Intenzitu epigenetických dějů ovšem můžeme ovlivňovat i my sami, zejména prostřednictvím svého životního stylu a výživy. Přitom je v naší moci nejen zabránit, aby negativní změny dále probíhaly, ale dokonce i vrátit mnohé z těch, které již proběhly.
Změny na buněčné úrovni
Epigenetické procesy přitom úzce zasahují i do buněčných mechanismů, které s aterosklerózou souvisejí. Zásadně například ovlivňují imunitní buňky jménem monocyty, které hrají při vzniku aterosklerózy stěžejní roli – právě z nich totiž vznikají makrofágy, které se posléze přeměňují na pěnové buňky tvořící jednu z hlavních složek aterosklerotického plátu. Epigenetické procesy také rozhodují o tom, zda z dalšího typu imunitních buně, tzv. naivních T-buněk, vznikne varianta Th-1, která podporuje vznik aterosklerózy, nebo Th-2, která před ní naopak chrání.
Epigenetické reakce se dotýkají i fungování buněk endotelu. Ovlivňují například aktivitu genu pro vznik enzymu eNOS, který je nezbytný pro tvorbu oxidu dusnatého – látky, která funguje jako vazodilatátor, tj. roztahuje cévy a ovlivňuje tak prokrvení tkání (právě produkce oxidu dusnatého je například zodpovědná za fungování Viagry). Pokud je enzym eNOS dysfunkční, podporuje to vznik aterosklerózy.
A v neposlední řadě epigenetické reakce ovlivňují i zánětlivé procesy v cévách, které s rozvojem aterosklerózy souvisejí. Jde například o produkci enzymu COX-2, který řídí tvorbu zánětlivých prostaglandinů.
A jakou roli v tom všem hraje tolik obávaný cholesterol? Ten samozřejmě výrazným rizikovým faktorem je, konkrétně pak ten s nízkou hustotou, označovaný jako LDL. Problém ale je, že samotná jeho hladina v krvi na míru rizika neukazuje – záleží totiž, jestli se vyskytuje ve formě větších částic, které tolik nebezpečné nejsou, nebo ve formě mnohem nebezpečnějších malých částic. Navíc platí, že aby se LDL stal nebezpečným, musí dojít k pozměnění jeho molekuly – typickým příkladem je oxidace způsobená volnými radikály.
7 kroků pro zdravé cévy
Jak už jsme zmínili výše, intenzitu epigenetických reakcí ve svém těle můžeme ovlivnit mnoha způsoby, zejména pak výživou a životním stylem. A týká se to i těch, které souvisejí s vývojem aterosklerózy a rizikem kardiovaskulárních onemocnění.
1. Rostlinné tuky vybírejte
Zároveň také neplatí, že rostlinné tuky jsou automaticky zdravé. A nezáleží přitom jen na úpravě – že smažení není zrovna dobrá volba, ví dnes už snad každý. Rostlinné tuky, pokud jsou za studena lisované, totiž sice obsahují esenciální nenasycené mastné kyseliny, které jsou pro zdraví srdce a cév zásadní, řada z nich má ale velice nevhodný poměr omega-3 a omega-6. Druhé jmenované jsou sice pro fungování našeho těla nezbytné, pokud ale ve stravě převažují, podporuje to průběh zánětlivých procesů v těle. Nevhodný poměr přitom mají nejen například slunečnicový či sójový olej, ale také například olej olivový – byť ten obsahuje polyfenoly, které srdci a cévám prospívají. Lépe je na tom olej řepkový a velmi příznivý poměr omega-3 a omega-6 najdete v konopném a lněném oleji.
2.Živočišné tuky s mírou
V posledních desetiletích docházelo v rámci prevence nemocí srdce a cév ke křížovému tažení proti živočišným tukům, což se ovšem ukázalo jako velká chyba. Je sice pravda, že jejich nadměrná konzumace je z epigenetického hlediska škodlivá, v rozumné míře ale mohou být spíše prospěšné. Obsahují sice cholesterol, ale jak už jsme řekli výše, nadměrná hladina této látky v krvi nám škodí pouze za určitých podmínek. Zcela eliminovat cholesterol ze stravy také není vhodné, protože tělo jej využívá například pro tvorbu steroidních hormonů. Živočišné tuky, pokud pocházejí od zvířat z farmářských chovů (volně se pasoucích), mají navíc vysoký obsah vitaminu K2, který je pro zdravé cévy nezbytný. Živočišné tuky tedy určitě z jídelníčku nevyřazujte, pouze snižte jejich celkový příjem a dávejte přednost živočišným produktům od volně se pasoucích zvířat – to platí pro mléčné výrobky, maso i vejce.
3.Omezte cukry
Do souvislosti se vznikem kardiovaskulárních chorob bývá často dávána spíše nadměrná konzumace živočišných tuků, nicméně platí, že možná ještě větší riziko představuje nadměrný příjem cukrů, zvláště pak těch s vysokým glykemickým indexem. Jednoduché cukry, pokud jejich příliš, totiž výrazně podporují průběh zánětlivých procesů v těle, a navíc podporují rozvoj inzulinové rezistence, tedy stavu, kdy tkáně ztrácejí citlivost na inzulin. Právě inzulinová rezistence přitom může vést nejen ke vzniku cukrovky, ale rovněž je výrazným rizikovým faktorem rozvoje endoteliární dysfunkce.
4.Jezte ovoce a zeleninu
Ovoce a zelenina jsou velmi bohaté na širokou škálu polyfenolů, které jsou nejen silnými antioxidanty, ale řada z nich má i výrazné epigenetické účinky, díky nimž například působí protizánětlivě, pomáhají snížit hladinu cholesterolu či krevní tlak.
5.Pravidelně se hýbejte
Nedostatek pohybu patří mezi 10 hlavních příčin všech nemocí. Fyzická aktivita, zejména ta aerobní, totiž pozitivně ovlivňuje průběh všech základních epigenetických reakcí, podporuje snížení tvorby prozánětlivých cytokinů, vede ke zvýšení vnitřního objemu srdce (jeho práce se tím stává efektivnější), k tvorbě nových cév (tzv. neoangiogeneze) a zvyšuje kapacitu organismu využívat glukózu, čímž snižuje její hladinu v krvi a brání rozvoji inzulinové rezistence. V rámci prevence kardiovaskulárních i jiných onemocnění se obvykle doporučuje 150 minut týdně aerobní aktivity v mírné až střední intenzitě (rozděleno minimálně do tří, lépe až do pěti dnů) doplněné o posilování. Vhodnou aerobní aktivitou přitom může být i svižnější chůze. 12 týdnů tréninku dokáže efektivně snížit metylaci DNA.
6.Zhubněte
Lidem s nadváhou či obezitou se to sice neposlouchá dobře, bohužel ale platí, že obezita je jeden z nejvýraznějších rizikových faktorů kardiovaskulárních nemocí. Nadměrný výskyt tukové tkáně s sebou totiž přináší zvýšenou míru zánětlivých procesů v těle, a obézní lidé navíc mají ve své DNA zvýšenou celkovou míru metylace, což je další rizikový faktor rozvoje nemocí srdce a cév.
7.Přestaňte kouřit
Tento nepříjemný zlozvyk výrazně zvyšuje míru metylace genů. To je hlavním důvodem, proč pro kuřáky významně stoupá riziko drtivé většiny civilizačních onemocnění, a ani ateroskleróza není výjimkou.
Vhodné doplňky stravy
Velice vhodnou součástí prevenci i léčby aterosklerózy jsou i doplňky stravy. Velmi efektivní mohou být zejména ty, které jsou nejen silnými antioxidanty, ale zároveň vykazují i epigenetické působení. Zde je malý výběr některých z nich.
Resveratrol
Na zdraví srdce a cév působí toto barvivo obsažené zejména v červeném víně hned několika cestami. Jde o silný antioxidant s protizánětlivými účinky. Efektivně přitom chrání před oxidací i LDL cholesterol. Ovlivňuje také tvorbu enzymů sirtuinů, stejně jako enzymu eNOS, který je nezbytný pro produkci oxidu dusnatého. Omezuje tvorbu řady prozánětlivých látek (např. NF-kB či TNF-α) i produkci látek s vazokonstrikčním účinkem (tj. uzavírajícím cévy). Resveratrol velmi vhodné kombinovat s komplexem oligomerních proantokyanidinů (OPC), což jsou silné antioxidanty s epigenetickými účinky, které jsou získávány z hroznových jadérek.
Coleus forskohlii
Bylinka pocházející z nižších poloh Himaláje je velice efektivní při snižování krevního tlaku. Působí totiž jako výrazný vazodilatant, tj. roztahuje cévy a zlepšuje tak zásobení tkání těla krví. Navíc podporuje hned několika cestami hubnutí.
Kurkumin
Má výrazný pozitivní vliv na metylaci genů i acetylaci histonů. Pomáhá snižovat LDL cholesterol a zvyšovat HDL cholesterol, zároveň má antiproliferativní efekt na monocyty a jde o velice silný protizánětlivý prostředek. A navíc efektivně podporuje hubnutí.
Vitamin K2
Důležitost této látky pro zdraví cév je zcela zásadní. Aktivuje totiž protein MGP, který čistí cévy od vápenatých usazenin. V rozsáhlé studii zkoumající 4500 mužů nad 55 let například vědci zjistili, že ti, kteří měli v krvi dostatečně vysokou hladinu vitaminu K2, měli o 52 % nižší riziko vzniku vápenatých usazenin, o 41 % nižší riziko vzniku kardiovaskulárních onemocnění a o 51 % riziko úmrtí na ně. Příjem K2 navíc působí nejen preventivně proti vzniku aterosklerotických plátů v cévách, ale zároveň dokáže rozpouštět již vzniklé usazeniny.
Omega-3
Tyto nenasycené mastné kyseliny mají výrazné epigenetické účinky, a to zejména v oblasti regulace metylace DNA. Dokáží vypínat geny zodpovědné za vznik zánětlivých procesů v cévní výstelce a tvorbu aterosklerotických plátů, a dokonce mohou zvrátit negativní epigenetické změny, jež vznikly v průběhu nitroděložního vývoje. Kromě toho snižují hladinu triglyceridů a LDL cholesterolu v krvi, snižují krevní tlak, tvorbu aterosklerotických plátů i riziko srdečních arytmií a žilní trombózy.
- Braunwald E. Cardiovascular medicine at the turn of the millennium: triumphs, concerns, and opportunities. N Engl J Med. 1997;337:1360–9.
- Libby P. Inflammation in atherosclerosis. Nature. 2002;420:868–74.
- Schroeder AP, Falk E. Vulnerable and dangerous coronary plaques. Atherosclerosis. 1995;118:S141–9.
- Ross R. Atherosclerosis – an inflammatory disease. N Engl J Med. 1999;340:115–26.
- https://www.wikiskripta.eu/w/Bu%C5%88ky_c%C3%A9vn%C3%ADho_endotelu
- van der Wal AC, Das PK, Bentz van de Berg D, et al. Atherosclerotic lesions in humans. In situ immunophenotypic analysis suggesting an immune mediated response. Lab Invest. 1989;61:166–70.
- Davenport P, Tipping PG. The role of interleukin-4 and interleukin-12 in the progression of atherosclerosis in apolipoprotein E-deficient mice. Am J Pathol. 2003;163:1117–25.
- Boesten LS, Zadelaar AS, van Nieuwkoop A, et al. Tumor necrosis factor-alpha promotes atherosclerotic lesion progression in APOE*3-Leiden transgenic mice. Cardiovasc Res. 2005;66:179–85.
- Caligiuri G, Rudling M, Ollivier V, et al. Interleukin-10 deficiency increases atherosclerosis, thrombosis, and low-density lipoproteins in apolipoprotein E knockout mice. Mol Med. 2003;9:10–7.
- Stenvinkel P, Karimi M, Johansson S, et al. Impact of inflammation on epigenetic DNA methylation – a novel risk factor for cardiovascular disease. J Intern Med. 2007;261:488–99.
- Sharma P, Kumar J, Garg G, et al. Detection of altered global DNA methylation in coronary artery disease patients. DNA Cell Biol. 2008;27:357–65.
- Hastings NE, Simmers MB, McDonald OG, et al. Atherosclerosis-prone hemodynamics differentially regulates endothelial and smooth muscle cell phenotypes and promotes pro-inflammatory priming. Am J Physiol Cell Physiol. 2007;293:C1824–33.
- Dje N’Guessan P, Riediger F, Vardarova K, et al. Statins control oxidized LDL-mediated histone modifications and gene expression in cultured human endothelial cells. Arterioscler Thromb Vasc Biol. 2009;29:380–6.
- Barker DJ, Winter PD, Osmond C, et al. Weight in infancy and death from ischaemic heart disease. Lancet. 1989;2:577–80.
- Lillycrop KA, Slater-Jefferies JL, Hanson MA, et al. Induction of altered epigenetic regulation of the hepatic glucocorticoid receptor in the offspring of rats fed a protein-restricted diet during pregnancy suggests that reduced DNA methyltransferase-1 expression is involved in impaired DNA methylation and changes in histone modifications. Br J Nutr. 2007;97:1064–73.
- Ait-Oufella H, Taleb S, Mallat Z, et al. Cytokine network and T cell immunity in atherosclerosis. Semin Immunopathol. 2009;31:23–33.
- Mallat Z, Taleb S, Ait-Oufella H, et al. The role of adaptive T cell immunity in atherosclerosis. Journal of Lipid Research. 2009;50:S364–9.
- Ansel KM, Lee DU, Rao A. An epigenetic view of helper T cell differentiation. Nat Immunol. 2003;4:616–23.
- Nencioni A, Beck J, Werth D, et al. Histone deacetylase inhibitors affect dendritic cell differentiation and immunogenicity. Clin Cancer Res. 2007;13:3933–41.
- Kawashima S, Yokoyama M. Dysfunction of endothelial nitric oxide synthase and atherosclerosis. Arterioscler Thromb Vasc Biol. 2004;24:998–1005.
- Cipollone F, Prontera C, Pini B, et al. Overexpression of functionally coupled cyclooxygenase-2 and prostaglandin E synthase in symptomatic atherosclerotic plaques as a basis of prostaglandin E(2)-dependent plaque instability. Circulation. 2001;104:921–7.
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3828841/#b77
- Fernández-Sanlés A, Sayols-Baixeras S, Subirana I, Degano IR, Elosua R. Association between DNA methylation and coronary heart disease or other atherosclerotic events: A systematic review. Atherosclerosis. 2017 Aug;263:325-333.
- Elisa Grazioli, Ivan Dimauro, Neri Mercatelli, Guan Wang, Yannis Pitsiladis,Luigi Di Luigi, and Daniela Caporossi. Physical activity in the prevention of human diseases: role of epigenetic modifications. BMC Genomics. 2017; 18(Suppl 8): 802.
- Soni KB, Kuttan R. Effect of oral curcumin administration on serum peroxides and cholesterol levels in human volunteers. Indian J Physiol Pharmacol. 1992;36:273–5.
- Ramirez Boscá A, Carrión Gutierrez M, Soler A, et al. Effects of the antioxidant turmeric on lipoprotein peroxides: implications for the prevention of atherosclerosis. AGE. 1997;20:165–8.
- Huang HC, Jan TR, Yeh SF. Inhibitory effect of curcumin, an anti-inflammatory agent, on vascular smooth muscle cell proliferation. Eur J Pharmacol. 1992;221:381–4.
- Susanne Voelter-Mahlknecht. Epigenetic associations in relation to cardiovascular prevention and therapeutics. Clin Epigenetics. 2016; 8: 4.
- Madhavi Jagtap, H. M. Chandola, and B. Ravishankar. Clinical efficacy of Coleus forskohlii (Willd.) Briq. (Makandi) in hypertension of geriatric population. Ayu. 2011 Jan-Mar; 32(1): 59–65.
- Gert Baumann, Stefan Felix, Ulrich Sattelberger, Gernot Klein. Cardiovascular Effects of Forskolin (HL 362) in Patients with Idiopathic Congestive Cardiomyopathy—A Comparative Study with Dobutamine and Sodium Nitroprusside. Journal of Cardiovascular Pharmacology 16(1):93-100 · August 1990
- Kate Rhéaume-bleue, B.Sc., N.D. Vitamin K2 and the Calcium Paradox. John Wiey & Sons Canada, 2012
- Gast GC, et al. A high menaquinone intake reduces the incidence of coronary heart disease. Nutr Metab cardiovasc Dis 2009 Sep 19(7):504-10; Beulens JW, ea al. High dietary manaquinone intake is associated with rediced coronary calcifiation. Atherosclerosis 2009 Apr, 203(2):489-93
- Schurgers L. Regression of warfarin-induced medial elastocalcinosis by high intake of vitamin K in rats. Blood 2007 Apr. 109(7):2823-31
- Caterina, R., & Massaro, M. (2005). Omega-3 Fatty Acids and the Regulation of Expression of Endothelial Pro-Atherogenic and Pro-Inflammatory Genes. J Membrane Biol Journal of Membrane Biology, 206(2), 103-116. Retrieved August 19, 2015
- Shirodkar AV, Marsden PA. Epigenetics in cardiovascular disease. Curr Opin Cardiol2011;26:209–15.
- Kris-Etherton PM, Harris WS, Appel LJ. Omega-3 Fatty Acids and Cardiovascular Disease New Recommendations from the American Heart Association. Arteriosclerosis, Thrombosis, and Vascular Biology. 2003;23(2):151-52.
Newsletter
PŘIHLASTE SE K ODBĚRU NOVINEK A MĚJTE VŽDY ČERSTVÉ INFORMACE